Il Premio Nobel per la Chimica è stato assegnato alle due ricercatrici Emmanuelle Charpentier e Jennifer A. Doudna “per avere sviluppato un sistema di editing del genoma”
Il sistema
di editing del genoma CRISPR/Cas9, sviluppato
dalle due ricercatrici, ha messo a
disposizione una nuova potente soluzione per cambiare il DNA degli animali,
delle piante e di altri microorganismi,
con una precisione senza precedenti.
Questo
sistema ha permesso negli ultimi anni di sviluppare nuove terapie contro i tumori e
potrebbe rendere possibile la cura di diverse malattie ereditarie.
Anche se
non ce ne rendiamo conto, da quando esiste la vita batteri e virus si fanno una guerra senza quartiere, dandosele di
santa ragione.
I batteriofagi (o
fagi), per esempio, sono particolari virus che vanno a caccia di batteri. Si
stima che da soli ogni giorno uccidano circa il 40% dei miliardi di miliardi di
batteri che vivono negli oceani (e se ne formano di nuovi miliardi
quotidianamente).
Dopo che
sono entrati in contatto con i batteri, i fagi
iniettano il proprio materiale genetico al loro interno, trasformandoli in
piccole fabbriche che produrranno altri virus, che a loro volta infetteranno
altri batteri. A differenza degli organismi più complessi e con un sistema immunitario avanzato, come il
nostro, i batteri hanno meno difese e falliscono quasi sempre a resistere.
Talvolta
accade però che alcuni batteri riescano a resistere all’attacco da parte dei
batteriofagi. Quando ciò avviene, salvano parte del materiale genetico del virus nel loro codice genetico, in una sorta di catalogo che i ricercatori
chiamano CRISPR, da clustered regularly interspaced short
palindromic repeats (brevi ripetizioni palindrome raggruppate e
separate a intervalli regolati).
Se in
seguito entra nuovamente in contatto con un virus, il batterio produce una
copia del materiale genetico che aveva archiviato e la passa a una proteina che
si chiama Cas9. Questa si mette al lavoro e cerca all’interno del batterio
pezzi di DNA e li confronta con quelli in archivio, per capire se sia presente
un virus.
Nel caso
in cui rilevi una corrispondenza, provvede a tagliare la sequenza genetica appartenente al virus, rendendola in questo modo
innocua. In mancanza di istruzioni chiare, il batterio non può essere
trasformato in una fabbrica di nuovi virus e non rischia di fare una brutta
fine.
Editing
La Cas9 è una proteina estremamente precisa nel tagliare pezzi di DNA.
Quando
Chapentier e Doudna se ne accorsero nel corso dei loro studi – mettendo insieme
le conoscenze raccolte separatamente in anni di ricerca e con altri ricercatori
– si chiesero se potessero sfruttare Cas9 per programmare il sistema CRISPR e
utilizzarlo per fare editing
del genoma (materiale genetico).
L’obiettivo
piuttosto ambizioso non le scoraggiò e portò alla creazione di un sistema di “forbici genetiche” descritto nel loro
studio pubblicato nel 2012.
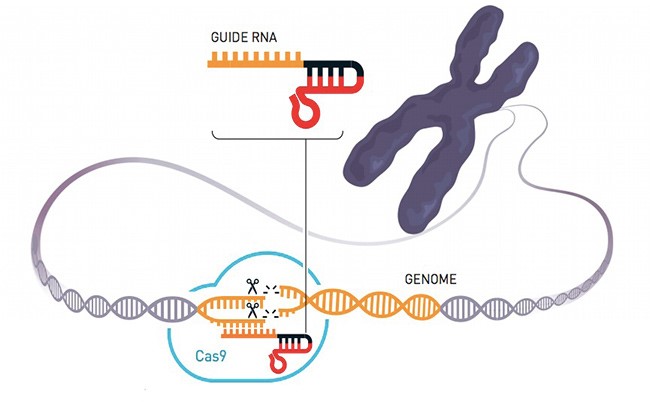
Semplificando
molto, le forbici di CRISPR/Cas9 per modificare il materiale genetico in una
cellula funzionano partendo da una sequenza genetica (RNA guida) approntata dai ricercatori che corrisponde a quella del
DNA dove si deve effettuare il taglio nella cellula.
La proteina Cas9 si mette
all’opera ed effettua il taglio: se non ci sono altre istruzioni, le cellula
ripara il proprio DNA perdendo un pezzo del proprio codice genetico,
comportando la perdita delle istruzioni per il gene che i ricercatori volevano
disattivare.
Il sistema
consente inoltre di innestare del nuovo DNA nella fase di riparazione, nel caso
in cui i ricercatori vogliano modificare ulteriormente il funzionamento della
cellula.
Opportunità
e pericoli
Prima
dell’avvento di CRISPR/Cas9, modificare i geni in una cellula era estremamente
difficile, richiedeva molto tempo e spesso portava a risultati poco affidabili.
Grazie
alle forbici genetiche, invece, si possono effettuare modifiche molto più
accurate e in tempi più rapidi.
Il sistema
è ormai diffuso in numerosi ambiti della ricerca, anche se non è sempre facile
da padroneggiare e ha mostrato di avere la necessità di qualche miglioramento.
I
ricercatori in questi anni hanno utilizzato CRISPR/Cas9 soprattutto per
comprendere meglio il funzionamento dei geni e le loro interazioni, per esempio
nel caso di malattie in alcuni animali.
La tecnica
è impiegata anche per modificare il genoma delle piante, in modo da renderle
più resistenti alla siccità, oppure a particolari parassiti, riducendo la
necessità di utilizzare composti chimici potenzialmente dannosi per la nostra
salute.
CRISPR/Cas9
è ritenuta inoltre una risorsa molto promettente per sviluppare nuove cure
contro alcune malattie ereditarie, anche se i risultati ottenuti per ora sono
ancora parziali e le tecniche da affinare. I ricercatori stanno anche
sperimentando l’impiego di CRISPR per modificare le nostre cellule immunitarie,
rendendole in grado di andare a caccia delle cellule tumorali con maggiore
efficacia.
Un sistema
così accurato di modifica del genoma apre inoltre scenari ancora inesplorati ed
eticamente controversi. In linea teorica, CRISPR/Cas9 potrebbe essere impiegato
per creare esseri umani geneticamente modificati. Potrebbe offrire enormi
benefici per ridurre i rischi di nascite con gravi malattie ereditarie, ma
potrebbe anche portare a modifiche irreversibili del nostro patrimonio
genetico, trasmesso di generazione in generazione.
Emmanuelle Charpentier è
nata nel 1968 a Jubisy-sur-Orge in Francia ed è direttrice della Divisione per
le scienze dei patogeni presso il Max Planck Institute di Berlino, in Germania.
Jennifer A. Doudna è nata
nel 1964 a Washington, DC (Stati Uniti) ed è docente presso l’Università della
California, Berkeley.