Un’arma potente per scongiurare una “DOPPIA PANDEMIA” di Covid/Influenza
Per diversi mesi, gli esperti della sanità globale hanno temuto una collisione tra il Covid-19 e l’influenza stagionale. Ma ora, con l’avvicinarsi della stagione influenzale e l’impennata del Covid-19, scongiurare una “doppia-pandemia” sembra più difficile del previsto.
Per di più, anche la “pigrizia pandemica” si è largamente diffusa, aumentando la riluttanza all’allontanamento sociale e all’uso delle mascherine. Allo stesso tempo, le nazioni sono afflitte da carenze e sfiducia nei confronti del vaccino anti-influenzale e, man mano che l’energia e la pazienza della popolazione nel seguire le norme diminuiscono, la tecnologia Novaeurus è diventata una difesa fondamentale in prima linea contro i due tipi di virus che causeranno disordine durante l’inverno: Sars-CoV-2 e l’influenza stagionale.
“C’è una notevole preoccupazione, mentre entriamo nei mesi autunnali e invernali e, conseguentemente, nella stagione influenzale, avremo quella temuta sovrapposizione di due malattie trasmesse dalle vie respiratorie”, avverte Anthony Fauci, M.D., Direttore dell’Istituto Nazionale statunitense di allergie e malattie infettive.
È necessario ricordare che il Covid-19 e l’influenza hanno in comune vari sintomi, come: febbre, tosse, dolori muscolari, affaticamento, mal di gola e mal di testa. Di conseguenza, l’insorgenza di questi sintomi causa un’ondata di ingressi al pronto soccorso, con una notevole incertezza sulla malattia da diagnosticare.
Potenzialmente si possono contrarre entrambe le malattie senza esserne a conoscenza e questo si configura come uno scenario decisamente preoccupante; per di più, adulti ospedalizzati che contraggono entrambe le malattie sono soggetti a un rischio mortale di 2/3 maggiore rispetto a chi contrae solo il Covid-19 (secondo Pubblic Health of England) e l’infezione influenzale sembra rendere i pazienti più vulnerabili a un attacco più grave di Covid-19. È dunque consigliabile, ove e quando possibile, sottoporsi alla vaccinazione anti-influenzale al fine di non congestionare le strutture sanitarie.
Sia l’influenza che Sars-CoV-2, possono diffondersi tramite le vie aeree ancor prima che sintomi compaiano e questi fattori indicano un unico imperativo per gli ospedali e le case di cura: assicurare una disinfezione continua dell’aria.
Le strategie di gestione dell’aria sono “importanti protezioni contro la diffusione delle infezioni all’interno delle strutture sanitarie” – asserisce il virologo australiano ed esperto di trasmissione influenzale, Ian Mackay, PhD.
Le stesse strategie, compresa la disinfezione dell’aria tramite la tecnologia NanoStrike® Novaeurus, possono essere implementate all’interno di ospedali, scuole, farmacie, uffici e ristoranti o, in qualsiasi spazio interno, anche con persone al loro interno, ove sono sicuramente presenti agenti patogeni infettivi. Le persone presenti all’interno di quello che possiamo definire un ambiente vivente, sono la più grande fonte di contaminazione. Essi rilasciano continuamente agenti patogeni nell’aria respirando, parlando, camminando, perdendo cellule epiteliali morte, starnutendo ecc. Per questo motivo, si verifica una costante fonte di contaminazione dell’ambiente, il che non può certamente dar vita a un ambiente sterile.
Se utilizzate 24/7, le unità di disinfezione dell’aria riducono le probabilità di trasmissione di Sars-CoV-2 e dell’influenza stagionale. Indipendentemente dal fatto che siano installati su una parete o uno scaffale, i dispositivi Novaerus funzionano in modo sicuro e discreto e, soprattutto, senza fare affidamento sull’intervento umano.
La tecnologia Novaerus è in grado di lavorare completamente in sicurezza 24/7, anche con persone presenti all’interno della stanza. Tuttavia, occorre ricordare che, gli ambienti a cui facciamo riferimento non sono ambienti “sigillati” – le correnti d’aria entrano ed escono dalla stanza per via delle finestre/porte portando con loro nuove fonti di contaminazioni esterne e compromettono potenzialmente la pulizia dell’aria appena trattata dal nostro dispositivo.
Ciò di cui dobbiamo ricordarci, è che Novaerus è una tecnologia per la mitigazione del rischio, in grado di ridurre costantemente la carica batterica presente nell’aria, trattandola 24/7 e limitando in tal modo il rischio di diffusione di un’infezione.
Come funziona la tecnologia al plasma a freddo NANOSTRIKE® NOVAERUS
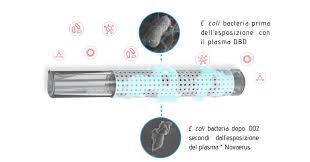
Questa tecnologia è una forma esclusiva di plasma atmosferico, a bassa energia, non termico (freddo) del tipo a scarica a barriera dielettrica (DBD) la quale non rilascia alcun tipo di ione ed è l’UNICA che disattiva i virus ed elimina batteri e funghi a livello del DNA. E’ in grado di distruggere i microorganismi di dimensioni nanometriche di diametro inferiore a 0.1 μm utilizzando una gamma di processi di inattivazione dei patogeni simultanei che si verificano nell’intervallo di tempo di nanosecondi; gli effetti distruttivi immediati che il Plasma ha sui patogeni a livello del DNA, UCCIDONO batteri e funghi, comprese le relative spore, e DISATTIVANO i virus. Tramite diversi processi chimico fisici si garantisce in 0,002 sec., un abbattimento fino al 99,99% di Virus, batteri, spore, funghi e allergeni.
Inoltre, poiché la tecnologia NanoStrike® offre processi di inattivazione multipli e simultanei, garantisce l’impossibilità per la resistenza antimicrobica (AMR) di svilupparsi nel tempo. La ricercaha infatti evidenziato la minaccia dello sviluppo della resistenza antimicrobica rispetto ai metodi di inattivazione singol